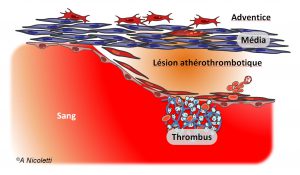
Les causes
Il existe un fossé entre phases cliniques précoces et essais pivots, creusé par l’absence de critères intermédiaires validés. L’imagerie moléculaire pourrait fournir de tels critères intermédiaires, combler ainsi ce fossé et être également utilisée pour des études mécanistiques.
Les essais cliniques sont chers, soulignant l’intérêt des essais randomisés fondés sur les registres qui sont à la fois moins chers et plus généralisables.
La prévention a été centrée sur les facteurs de risque classiques en négligeant d’autres facteurs telles que les apnées obstructives du sommeil et la mauvaise santé bucco-dentaire. Il s’agit pourtant de déterminants fréquents, potentiellement importants de l’athérothrombose, et de possibles nouvelles cibles thérapeutiques.
Ce que nous voulons faire
Un registre français multicentrique continu de l’infarctus du myocarde
Il sera lié aux bases de données (dont le SNIIRAM) permettant un suivi automatisé à faible coût des événements cliniques et de la consommation de soins. Il permettra des études prospectives et des essais randomisés nichés dans un registre. Il sera pérennisé grâce aux financements d’essais pivots ultérieurs, au travers notamment de collaborations européennes.
Améliorer la sélection des patients pour les traitements
Par des outils d’évaluation du risque, à l’imagerie et aux biomarqueurs.
Développer des ligands et des méthodes d’imagerie moléculaire de l’athérothrombose
Pour tester l’effet de nouveaux traitements, identifier a) l’origine de la thrombose dans les accidents vasculaires cérébraux ischémiques idiopathiques ; b) les plaques vulnérables susceptibles de progresser ; et aider au ciblage des patients pour les traitements nouveaux mais chers.
Comorbidités
Avec ces outils, étudier l’association et l’impact de la mauvaise santé bucco-dentaire et des apnées du sommeil sur l’athérothrombose dans la population générale et après infarctus du myocarde. Deux aspects clés sont la réalisation d’essais randomisés pour évaluer l’efficacité des traitements de ces comorbidités sur l’athérothrombose, et la dissémination de nos résultats aux professionnels de santé et au grand public.
Contexte et rationnel
L’athérothrombose est le processus physiopathologique qui sous-tend aux infarctus du myocarde (IM) et aux accidents vasculaires cérébraux, les deux premières causes de décès dans le monde. Des progrès importants ont été réalisé pour leur prévention et leur traitement. Cependant, en dépit des progrès réalisés, ces maladies restent très répandues et constituent une source majeure de morbi-mortalité, d’invalidité et font peser des coûts élevés sur notre société. Pour les patients qui survivent à un événement initial, le risque résiduel est encore élevé (par exemple, la mortalité toutes causes à 5 ans est d’environ 20% après un IM). De plus, on note un ralentissement sensible des progrès, comme en témoignent les échecs de plusieurs essais randomisés récents (p. Ex. Aim-High, HPS-2, Solid, Stability, Illustrate, Accelerate, Dal-Outcomes) qui ont inclus plus de 100 000 patients pour un coût énorme.
Plusieurs facteurs entravent notre progression :
L’athérothrombose est un processus lent, silencieux et complexe, évoluant de façon asymptomatique pendant plusieurs décennies avant tout événement. Il peut causer un événement abrupt et parfois mortel avec peu ou pas de symptômes prémonitoires. Jusqu’à présent, le diagnostic de l’athérothrombose repose sur l’imagerie morphologique, qui se concentre sur l’identification du rétrécissement des artères par des plaques athéromateuses. Malheureusement, la majorité des événements thrombotiques aigus sont causés par des plaques peu «vulnérables», qui provoquent un rétrécissement minimal du vaisseau et qui subissent une rupture ou une érosion, provoquant une thrombose et une occlusion aiguë de l’artère. Par conséquent, il est essentiel de développer l’imagerie moléculaire pour permettre l’identification des plaques vulnérables, propices à la rupture, ainsi que de délimiter les différents stades et composants de la maladie, et leur activité métabolique, étant donné que les «plaques actives» sont plus susceptibles de devenir vulnérables et doivent donc bénéficier d’une thérapie plus intensive et/ou prolongée. Une imagerie spécifique pour des plaques complexes ou des biomarqueurs spécifiques pourrait aider à proposer aux patients des thérapies nouvelles et plus coûteuses (p. Ex. des inhibiteurs de PCSK9)
Chez les patients atteints d’AVC ischémique, aucune cause définie ne peut être identifiée chez 40% des patients. Nous avons déjà prouvé que la rupture et la thrombose subséquente des lésions non sténotiques dans les artères carotides peuvent provoquer un AVC ischémique (Hyafil et al., Circulation 2014; 129: 130-1). Les plaques rompues sont cependant difficiles à identifier puisqu’elles peuvent être localisées n’importe où dans l’aorte thoracique (Amarenco et al., N Engl J Med 1992, 326: 221-225, The French Study of aortic Plaques in Stroke Group. 1996, 334: 1216-21), le long des troncs supra-aortiques (Hyafil et al., Eur. J Nucl Med Mol Imaging.2016; 43: 270-9), jusqu’aux artères intracrâniennes (Klein et al., Neurology 2006; 67: 327-9). Une meilleure détection de ces plaques coupables permettrait un diagnostic plus précis pour les patients souffrant d’AVC ischémique ainsi qu’une meilleure sélection de traitements pour la prévention des événements ischémiques récurrents.
Dans le développement d’agents pour prévenir les événements athérothrombotiques tels que les infarctus du myocarde ou l’AVC, il y a un fossé entre le développement clinique précoce et les essais pivots de phase III car il n’y a pas de marqueurs intermédiaires validés d’issue clinique qui pourraient être testés dans les essais de phase II. Cela souligne la valeur potentielle de l’imagerie moléculaire de l’athérothrombose, qui peut être utilisée pour les études mécanistiques et comme marqueur intermédiaires de l’initiation et de la progression de la maladie.
En raison de l’écart entre le développement clinique précoce et les essais cliniques de phase III, il est difficile de développer et de tester de nouveaux traitements car cela implique d’investir plusieurs centaines de millions de dollars pour chaque composé à tester ; en effet, la taille les essais de phase III dans le domaine de l’athérothrombose requièrent des effectifs très importants (souvent plus de 15 000 patients). En outre, les participants aux essais randomisés sont souvent très sélectionnés et ne sont pas représentatifs de la pratique clinique courante. Cela met l’accent sur la valeur des essais randomisés nichés dans les registres qui fournissent des données pouvant être extrapolés plus facilement à la population générale et à une fraction du coût des essais classiques.
Ce manque de compétitivité provient sans doute d’un manque d’organisation collective. Ainsi, la France joue un rôle qui décline dans le développement de nouvelles thérapies cardiovasculaires. Le développement du réseau de recherche universitaire est essentiel pour améliorer la performance française.
Par exemple, en développant des interventions antithrombotiques avec un rapport efficacité / sécurité optimisé ou en améliorant la sélection des candidats pour les schémas thérapeutiques complexes antithrombotiques («personnalisation des thérapies»), à l’aide de biomarqueurs, d’outils d’évaluation des risques ou d’imagerie.
La prévention s’est concentrée sur la prise en charge des facteurs de risque conventionnels (hypertension, hypercholestérolémie, diabète), négligeant les comorbidités importantes tels que des troubles respiratoires du sommeil et la mauvaise santé bucco-dentaire. Il existe une incertitude quant à savoir si ces comorbidités sont causales dans l’athérothrombose ou simplement cofacteurs. Cette question est cruciale : si le risque cardiovasculaire associé à ces comorbidités très fréquentes est modifiable, cela pourrait ouvrir de nouvelles voies de prévention et de traitement, à un moment où l’efficacité des approches conventionnelles anti-thrombotiques et hypolipémiantes ne progresse plus.